骨盆骨折(fracture of the pelvis,FP)是一种因高能暴力或骨质疏松症所引起的两侧髋骨和前部耻坐骨支与骶骨的严重损伤。由于骨盆解剖结构复杂,位置特殊且骨折类型多样,手术复位内固定是FP的常用治疗手段,其临床治疗目标为骨折断端解剖复位、重建关节面及提供稳定的固定措施[1]。骨盆骨折可能发生多种并发症[2],因此骨盆骨折的手术、护理及康复一直是巨大挑战。
近年来,快速康复外科(enhanced recovery after surgery,ERAS)作为一种新的临床理念形式,通过整合和优化麻醉方式、围术期处理、疼痛管理和康复训练等各项措施,以减少创伤侵袭并减轻手术引起患者的压力反应,ERAS的核心是加速患者术后的康复。目前已被用于治疗许多骨科疾病[3,4]。因此本研究通过将ERAS理念应用于骨盆骨折手术复位固定治疗,并探讨其临床疗效和应用价值。
1 材料与方法
1.1 一般资料
选取2017年2月至2019年1月间在我院骨科收治的骨盆骨折患者病例资料进行分析,依据入选和排除条件,共纳入97例患者,按照随机数表法分为观察组和对照组。其中观察组共纳入患者52例,男性22例,女性30例,年龄范围为(19~74)岁,平均年龄为(47.3±17.4)岁;对照组共纳入患者45例,男性16例,女性29例,年龄范围为(17~82)岁,平均年龄为(51.7±24.3)岁。两组患者性别、年龄无统计学差异(P>0.05),详细临床资料见表1。所有受试者均符合以下入选条件:①经病史、临床表现及X线或CT影像学扫描证实为骨盆骨折,且符合手术切除指征者;②患者自身情况良好,无心、肺、肾功能障碍,麻醉评分在ASAⅠ~Ⅲ级可耐受手术麻醉者;③骶髂关节脱位超过1 cm者;④髂骨、骶骨骨折移位明显,且耻骨联合分离超过3 cm;⑤患者及其家属依从性良好,对入组情况充分知情了解,可接受定期随访者。排除条件:①既往有慢性糖尿病、缺血性心肌病、脑血管疾病病史或术前合并有重症感染及休克者;②合并精神系统疾病,如语言表达障碍或意识不清者。
表1 两组患者详细临床资料
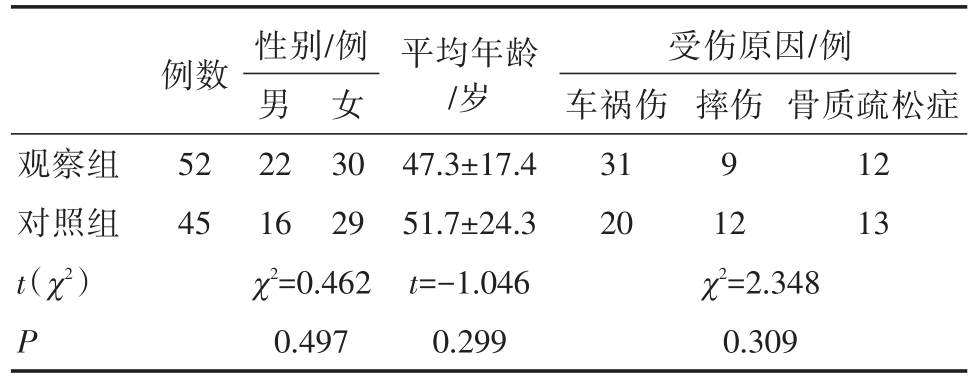
观察组对照组t(χ2)P例数52 45性别/例男22 16 χ2=0.462 0.497女30 29平均年龄/岁47.3±17.4 51.7±24.3 t=-1.046 0.299受伤原因/例车祸伤31 20 χ2=2.348 0.309摔伤9 12骨质疏松症12 13
1.2 方法
1.2.1 观察组治疗方案 观察组患者围术期治疗措施均遵循ERAS理念[5],具体方案如下:①术前宣教:主管医生充分了解患者病情,告知管床医生及责任护士名字,麻醉师于择期手术1天前访视患者,向患者及其家属简要介绍手术室环境和手术流程,降低患者因环境更换所引发的焦虑和不安;同时了解患者近期思想波动,拟定个性化心理疏导,降低负性心理情绪所引发的应激反应;②术前功能锻炼:择期手术1周前即开始对身体恢复功能进行锻炼,利用适度的有氧运动,如爬楼梯、吹气球等方式训练患者的心肺功能;责任护士与术前2天指导患者正确咳嗽方法以及训练床上大小便能力,促进患者尽早适应术后状态;③胃肠道准备:患者于择期手术前3d给予肠内营养剂代替普通饮食,术前1 d给予聚乙二醇电解质散导泻行胃肠道准备,术前6 h禁食固体食物但无需禁饮,术前2 h可分次给予患者温热10%葡萄糖溶液250 mL口服,每次50 mL,有利于缓解患者饥饿、口渴以及紧张等不适,同时补充能量,避免术中发生低血糖,减轻手术操作所带来的应激反应。另外术前不常规留置胃肠减压管和导尿管;④麻醉管理:术中应用连续性硬膜外神经阻滞联合全身麻醉方式进行处理,选择患者T8~9棘突间隙穿刺进针置管,给予1%利多卡因行硬膜外神经阻滞。待麻醉平面显现后,舒芬太尼(0.5 μg/kg)、咪达唑仑(0.1 mg/kg)、丙泊酚(2 mg/kg)以及复合吸入性七氟烷联合诱导并维持麻醉,间断给予顺阿曲库胺(2 mg/kg)松弛肌肉,术中严格限制液体总量,维持出入量平衡;⑤术中保温:术中严格把控手术室内温度,维持在25℃~30℃之间,手术台上放置保温水毯,液体输注过程中进行加温处理,持续监测体温波动,避免低体温发生;⑥术后疼痛护理:术后可安装止痛泵,并根据疼痛评分在护理人员指导下使用,以减轻疼痛应激反应;⑦早期进食:患者自麻醉清醒后6 h开始,每隔12 h可给予10%葡萄糖溶液100 mL缓慢口服,预防低血糖症状并刺激胃肠道蠕动;⑧早期功能锻炼:术后1~2 d尝试在床上进行四肢活动,练习深呼吸、咳嗽等动作,术后3 d练习床上坐起,术后4~7 d练习在床边站立并逐步过渡至下床行走;⑨盆腔引流管护理:术后每天观察引流液颜色和性质,严格记录引流量,保证引流管通畅,做好无菌护理,术后5~7 d尽早拔除。
1.2.2 对照组治疗方案 对照组患者围术期给予常规外科处理措施,方案如下:①术前1天常规访视患者,仅告知患者手术流程,不针对患者实施个性化心理疏导和术前功能训练;②手术前3天告知患者停止进食固体食物,术前1d和手术日行肠道灌洗,术前12 h禁食,6 h禁饮,且手术当日常规留置胃肠减压管和尿管;③术中仅采用无菌巾覆盖的方法进行保暖,不常规应用水毯和液体加热器;④术后早期禁食水,待肛门排气后拔出胃肠减压管,肠道功能恢复后给予流质饮食;⑤术后不主动给予镇痛控制,待患者疼痛无法忍受时给予肌肉注射止疼药物;⑥根据患者自身意愿进行活动,不要求早期功能锻炼,术后12~14 d拔出盆腔引流管。
1.3 疗效评估
1.3.1 疼痛等级评分 采用痛觉可视化评分(visual analogue scale,VAS)对两组患者治疗前及麻醉苏醒后12 h的主观疼痛等级进行模拟评价[6]。评分系统中将疼痛分为10个等级,其中“0”表示无自觉疼痛,“10”表示难以忍受的剧痛,中间不同分值按照次序分别代表不同程度的疼痛水平。患者根据自身症状在评分尺中模拟疼痛分值,临床镇痛评定中以0~2为优,3~5分为良,6~8分为可,9~10分为差,计算镇痛有效率=(优+良)/总例数×100%,详见图1。
1.3.2 临床指标观察 两治疗组术中自麻醉终止至患者苏醒所历经的时间记录为苏醒时间。观察两组患者术中出血量、苏醒时间、排气时间、下床时间、住院时间和骨折愈合时间水平。其中临床判定骨折愈合标准[7]为:①患侧肢体局部无压痛及纵向叩击痛;②X线下显示骨折断端恢复良好,骨折线模糊,有连续骨痂形成;③患者可自行完成简单动作,局部无异常活动。对比两组患者机体功能恢复时间变化。记录两组患者围术期治疗过程中相关性并发症情况。
1.3.3 骨盆功能恢复 采用Majeed评分标准[8]对治疗后3个月的骨盆功能进行评价。在评分量表中包含疼痛(30分)、工作(20分)、坐(10分)、站立(36分)和性生活(4分)等5个方面;在临床评定中,满分为100分,其中超过85分为优,70~85分为良,55~69分为可,小于55分为差,骨盆功能恢复率=(优+良)/总例数×100%。
1.4 统计学分析
应用SPSS 20.0软件进行统计学分析。疼痛等级评分、术中出血量、苏醒时间、下床时间、住院时间及骨折愈合时间为计量型数据,以x±s表示,组间比较采用t检验,相关性并发症和骨盆功能恢复情况为计数型数据,采用χ2检验,P<0.05为有统计学差异。
2 结果
2.1 疼痛等级改变
治疗前观察组疼痛模拟评分为(5.7±1.4)分,对照组为(6.1±0.7)分,两组比较无统计学差异(t=-1.668,P=0.099,表2);麻醉苏醒后12 h,观察组疼痛等级水平为(2.4±1.1)分,对照组为(4.7±2.3)分,两组间差异有统计学意义(t=-5.588,P<0.001)。观察组治疗前与麻醉苏醒后12 h疼痛评分水平比较,差异有显著统计学意义(t=11.724,P<0.001,图1),对照组两时间监测点比较,差异无统计学意义(t=0.598,P=0.072)。其中观察组中镇痛有效率为88.5%(46/52),对照组为64.4%(29/45),组间差异有统计学意义(χ2=7.935,P=0.005)。
表2 两组患者治疗前及麻醉苏醒后12 h疼痛等级水平改变(x±s)
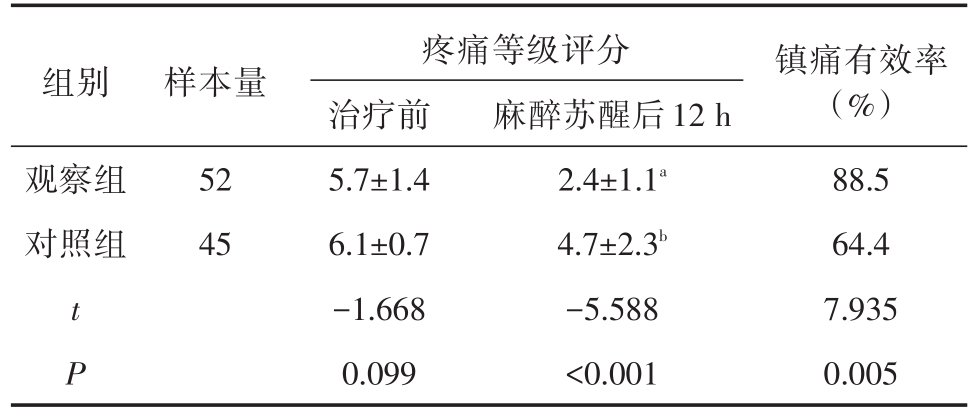
a,b分别表示麻醉苏醒后12 h与治疗前比较,t=11.724,P<0.001;t=1.124,P=0.093
组别 样本量观察组对照组52 45 t P疼痛等级评分治疗前5.7±1.4 6.1±0.7-1.668 0.099麻醉苏醒后12 h 2.4±1.1a 4.7±2.3b-5.588<0.001镇痛有效率(%)88.5 64.4 7.935 0.005
2.2 临床观察指标变化
观察组术中出血量(143.7±41.6)mL与对照组(126.5±53.1)mL比较,差异无统计学意义(t=1.783,P=0.078);观察组麻醉后苏醒时间(5.7±2.4)min较对照组(13.1±4.7)min明显缩短;观察组排气时间、下床时间及住院时间均较对照组提前,差异具有统计学意义(P<0.05,表3);对治疗后骨折愈合时间结果进行比较,两组间差异无统计学意义(t=1.138,P=0.258,表4)。
表3 两组患者临床观察指标改变(x±s)
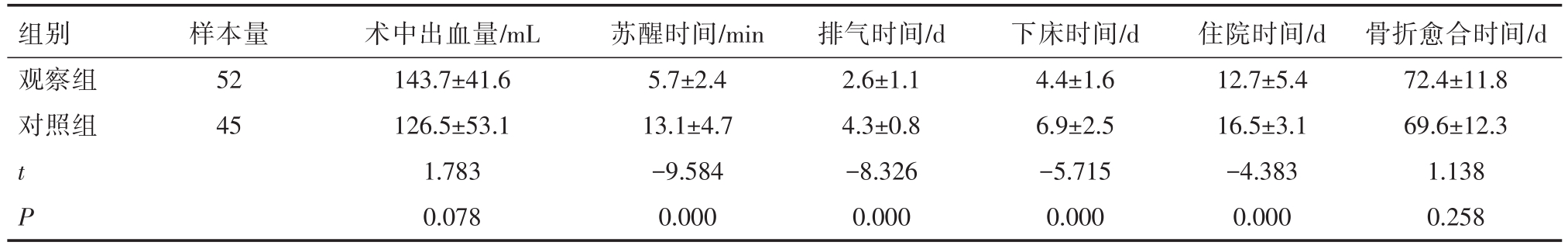
组别观察组对照组样本量52 45 t P术中出血量/mL 143.7±41.6 126.5±53.1 1.783 0.078苏醒时间/min 5.7±2.4 13.1±4.7-9.584 0.000排气时间/d 2.6±1.1 4.3±0.8-8.326 0.000下床时间/d 4.4±1.6 6.9±2.5-5.715 0.000住院时间/d 12.7±5.4 16.5±3.1-4.383 0.000骨折愈合时间/d 72.4±11.8 69.6±12.3 1.138 0.258
2.3 相关性并发症情况
治疗过程中,观察组患者围术期相关性并发症例数为12例,对照组为47例。其中对照组尿路感染、肺炎、低体温及恶心呕吐等症状发生例数明显高于观察组(P值分别为 0.006、0.034、0.000、0.018);两组患者中,下肢深静脉血栓发生例数比较,无统计学差异(P=0.241,表4)。
表4 两组患者围术期治疗相关性并发症情况(例)
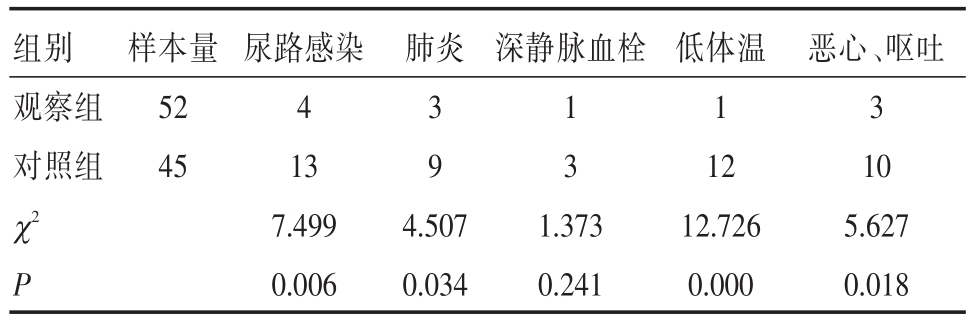
组别观察组对照组样本量52 45肺炎 深静脉血栓尿路感染4 13 7.499 0.006 3 1 1 931 4.5071.37312.7 χ2 P 0.0340.241低体温2 26 0.000恶心、呕吐3 10 5.627 0.018
2.4 骨盆功能恢复情况
治疗后3个月,观察组骨盆功能恢复为优的患者共31例,良为12例,可为7例,差为2例,其功能恢复率为82.7%;对照组中恢复为优的患者共20例,良为16例,可为6例,差为3例,其功能恢复率为80.0%。两治疗组中功能恢复情况经χ2检验提示,差异无统计学意义(χ2=2.730,P=0.435,表4)。
表5 两组患者骨盆功能恢复情况(例)
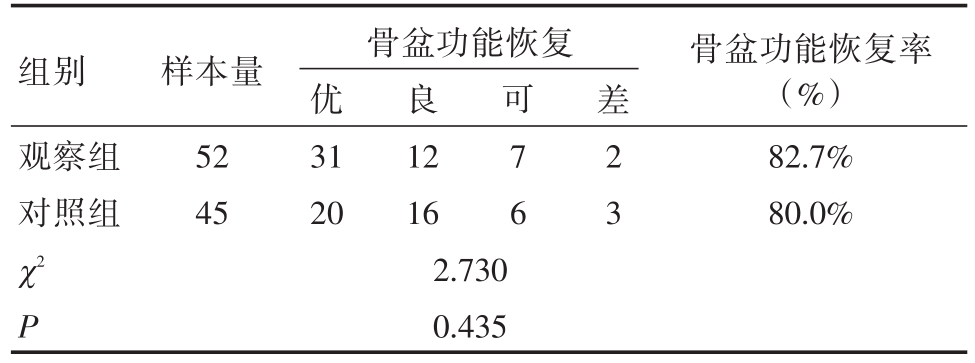
组别观察组对照组样本量52 45良12 16骨盆功能恢复优31 20 2.730 0.435可7 6差2 3骨盆功能恢复率(%)82.7%80.0%χ2 P
3 讨论
加速康复外科理念(ERAS)是一种多模式、多学科综合的标准化康复方案。丹麦医生Kehlet[9]首次提出ERAS概念,认为单一的处理措施无法有效改善外科围手术期并发症发生现状,因此提倡通过优化围手术期管理,改良传统麻醉常规措施,利用多镇痛方式联合并结合心理学干预、个体化心理疏导以及早期功能恢复锻炼,从而降低身体和心理因手术创伤所引起的应激性反应,达到降低术后并发症、缩短住院时间和促进患者快速恢复的临床目的。目前,欧洲ERAS协会已在结直肠手术、胰十二指肠手术等腹部外科操作中制定相关康复指南,并在临床应用中取得显著的疗效[10-12]。近年来,有报道[4,13]表明,ERAS 理念可减少骨科手术住院时间和术后并发症。
本研究在ERAS理念下指导骨盆骨折的围术期治疗,结果显示术前与患者充分沟通,通过个性化心理疏导方式营造良好的医患关系,对缓解患者因心理、知识误区所引起的陌生、紧张等负面情绪起积极作用;另一方面,医生与患者共同制订治疗及术后恢复方案,可使患者在治疗过程中获得更多参与感,促使其尽快适应术后状态。现阶段,外科手术前是否需要常规清洁灌肠和绝对禁食12 h以上是目前存在争议的焦点[14]。传统外科理念认为,术前清洁灌肠能有效减少感染的发生,择期手术患者从术前1晚即开始禁食可在最大程度上降低术中反流、误吸的风险。但Kobayashi等[15]认为术前机械灌肠会加重患者术中肠道应激,导致术后肠麻痹发生几率增加。同时,有研究[16]指出,术前较长时间的禁食状态可增加机体胰岛素抵抗,并促进胰高血糖素及皮质醇的释放,增加机体对蛋白质的分解作用及患者不适感。本研究遵循ERAM理念,术前不采取常规清洁灌肠和严格禁食,术前2 h可给予葡萄糖溶液口服,维持患者机体高血糖水平,有利于缓解患者饥饿、口渴以及紧张等不适,补充能量避免术中发生低血糖,减轻手术操作所带来的应激反应;术后提倡早期经口进食,在保证能量供应的同时,刺激机体功能恢复,患者肛门排气时间、下床时间及住院时间均较常规外科围术期管理方式显著提前。
另外,本研究术中麻醉方案采用全身麻醉联合硬膜外神经阻滞的方式进行处理,结果表明麻醉过程中,联合镇痛方案麻醉后,患者苏醒时间较常规麻醉方式提前。硬膜外神经阻滞可阻断脊神经传入刺激,降低交感神经及肾上腺皮质应激性反应,在联合丙泊酚和吸入性麻醉药诱导全身麻醉的同时,有助于减少阿片类镇痛剂的应用,降低和预防麻醉后出现剧烈恶性和呕吐(PONV)的风险,可在调节麻醉深度以及促进患者苏醒和恢复认知功能方面具有较好的临床效果[17]。术后采取加用自控式镇痛泵(PCA)的多模式镇痛方案,术后患者腹部镇痛效果明显优于常规方案,因此可改善患者因疼痛而无法主动呼吸、咳嗽等状态,从而降低肺部感染的并发症风险。
不仅如此,在ERAS理念指导下,严格限制液体出入量平衡和维持术中适宜体温对于患者术后快速康复至关重要。有研究[18]指出,晶体液的过量输入可显著增加肺部感染以及术后肠梗阻的风险,而低体温则更易引起伤口感染、血小板功能障碍、免疫功能降低以及心脏并发症。本研究发现,常规麻醉方案中患者中心静脉压随麻醉时间逐渐升高,对心脏损伤的风险明显高于ERAM管理方案。同时,ERAM管理方案可平稳维持术中体温,增加患者对术中应激的耐受能力。
综上,快速康复麻醉管理理念打破了常规观念的限制,是一种多学科协作的高质量临床麻醉管理方案。ERAM通过联合个性化心理学疏导以及多模式镇痛方式,有效降低了胃肠外科手术中的创伤应激反应,降低术后并发症发生率,在促进患者早期功能恢复方面疗效良好。
参考文献
[1] Bernhard JT,Mark G,Victor N,et al.Stress fracture of the pelvis and lower limbs including atypical femoral fractures-a review[J].Insights Imaging,2015,6(1):97-110.
[2] Kobziff L.Traumatic pelvic fractures[J].Orthop Nurs,2006,25(4):235-241.
[3] Ljungqvist O,Scott M,Fearon KC.Enhanced Recovery After Surgery:A Review[J].JAMA Surg,2017,152(3):292-298.
[4] Zhu S,Qian W,Jiang C,et al.Enhanced recovery after surgery for hip and knee arthroplasty:a systematic review and metaanalysis[J].Postgrad Med J,2017,93(1106):736-742.
[5] 候宝莲.快速康复外科在腹部外科手术护理中的应用进展[J].中华损伤与修复杂志(电子版),2019,14(3):235-237.
[6] Andy WKY,Natelie SMW.The Historical Roots of Visual Analog Scale in Psychology as Revealed by Reference Publication Year Spectroscopy[J].Front Hum Neurosci,2019,13:86.
[7] 王保仓,张立峰,于永林,等.骨折愈合研究进展[J].局解手术学杂志,2003,12(5):374-376.
[8] 刘盾,李磊,陈兴春,等.3D打印体外建模辅助微创治疗复杂骨盆骨折[J].局解手术学杂志,2019,28(1):57-60.
[9] Kehlet H.Multimodal Approach to Control Postoperative Pathophysiology and Rehabilitation[J].Br J Anaesth,1997,78(5):606-617.
[10] Lassen K,Soop M,Nygren J,et al.Consensus Review of Optimal Perioperative Care in Colorectal Surgery:Enhanced Recovery After Surgery(ERAS)Group Recommendations[J].Arch Surg,2009,144(10):961-969.
[11] Passeri M,Lyman WB,Murphy K,et al.Implementing an ERAS Protocol for Pancreaticoduodenectomy Does Not Affect Oncologic Outcomes when Compared with Traditional Recovery[J].Am Surg,2020,86(2):e81-e83.
[12] 李月春,王东霞,李菜诗,等.快速康复外科理念在结直肠肿瘤围术期中的应用研究[J].岭南现代临床外科,2013,13(4):301-304.
[13] Wainwright TW,Immins T,Middleton RG.Enhanced recovery after surgery:An opportunity to improve fractured neck of femur management[J].AnnRCollSurgEngl,2016,98(7):500-506.
[14] 冷希圣,韦军民,刘连新,等.普通外科围手术期疼痛处理专家共识[J].中华普通外科杂志,2015,30(2):166-173.
[15] Kobayashi S,Ooshima R,Koizumi S,et al.Perioperative Care with Fast-Track Management in Patients Undergoing Pancreaticoduodenectomy[J].World J Surg,2014,38(9):2430-2437.
[16] Nygren J,Soop M,Thorell A,,et al.Preoperative oral carbohydrate administration reduces postoperative insulin resistance[J].Clin Nutr,1998,17(2):65-71.
[17] Feldheiser A,Aziz O,Baldini G,et al.Enhanced Recovery After Surgery(ERAS)for gastrointestinal surgery,part 2:consensus statement for anaesthesia practice[J].Acta Anaesthesiol Scand,2016,60(3):289-334.

