

岭南现代临床外科 ›› 2020, Vol. 20 ›› Issue (01): 21-24.DOI: 10.3969/j.issn.1009-976X.2020.01.005
摘要:
肝脏上皮样血管内皮瘤(hepatic epithelioid he-mangioendothelioma,HEHE)是一种非常罕见的血管源性恶性肿瘤,其生物学行为不确定[1]。由于HEHE的罕见性,非特异性症状和外科医生、放射科医师缺乏经验使得该肿瘤的诊断非常具有挑战性,故术前诊断非常困难,HEHE容易被误诊为其他原发或继发肿瘤。现回顾性分析1例经病理证实的肝脏上皮样血管内皮瘤,旨在提高对该肿瘤的认识。
患者,男,34岁。患者因“右侧腰背部间歇性胀痛1月,检查发现右肾上腺肿块9天”于2017年10月9日在当地医院入院。现病史:患者无明显诱因出现右侧腰背部胀痛不适,疼痛呈间歇性发作,劳累后明显,休息可缓解,无尿频、尿急、尿痛,无肉眼血尿,无畏寒、发热,无腹胀、腹痛,1月后于9月30日到当地医院就诊,行腹部超声检查示“右肾上腺区囊性包块(大小21 mm×17 mm,后方回声增强)”,于10月1日进一步行CT平扫+增强报告“右侧肾上腺囊实性结节,大小28 mm×20 mm×15 mm,增强扫描实性部分明显强化,囊性部分轻度强化,边界清楚,性质待定,囊腺瘤可能性大,右肾上极小囊肿,肝内胆管轻微扩张。当时医师建议患者到上级医师进一步诊治。患者为求进一步诊治收入我院。患者自起病以来,精神、食欲、睡眠尚可,大便如常,体重无明显变化。既往史:诊断“乙肝”21年,既往有药物治疗(具体不详),2~3年前诊断有“胸膜炎”经药物治疗已痊愈(具体不详),有“浅表性胃炎、肠息肉”病史多年,否认“高血压、糖尿病、心脏病”病史,否认有“结核、痢疾”等其它传染病史,否认食物及药物过敏史。否认重大外伤史、手术史,否认输血史,否认口服抗凝药史。其他其他系统回顾未见异常。个人及家族史:吸烟11~12年,平均1包/日,偶尔饮酒,不酗酒。无长期工业毒物,粉尘,放射性物质接触史。否认不洁性交史。否认家族中遗传性疾病、恶性肿瘤及精神疾病史。初步诊断为诊断:①右肾上腺占位性质待查;②乙肝。
入院查体:体温:36.0℃,脉搏:80次/分,呼吸:18次/分,血压:120/80 mmHg。腹平软,肝脾未及,Murphy's征(-)。肝上界位于右锁骨中线第5肋间。腹部叩诊鼓音,肝、脾区无叩痛,移动性浊音(-),肠鸣音正常。脊柱无畸形,活动正常。双下肢无浮肿,生理反射存在,病理反射未引出。专科检查结果如下:双肾区无红肿隆起,双肾肋下未及,双肾区无叩痛,双肾区未闻及血管杂音。双侧季肋点无压痛,输尿管全程无压痛,膀胱区无膨隆,无压痛,无及肿块。外生殖器未见异常。
实验室检查结果:乙肝DNA定量:乙型肝炎病毒8.88×104IU/mL;乙型肝炎病毒表面抗原阳性(+),乙型肝炎病毒e抗体弱阳性(±),乙型肝炎病毒核心抗体阳性(+),乙型肝炎病毒前S1抗原阳性(+),诊断“乙型病毒性肝炎(活动期)”;凝血常规:纤维蛋白原1.50 g/L;尿常规、生化、肿瘤性指标等未见明显异常。肾上腺皮质节律、醛固酮、促肾上腺皮质节律等检查未见明显。
上腹部CT平扫+增强影像报告如下:右侧肾上腺区见一类圆形结节,大小约25 mm×19 mm,边界清,平扫内见一囊状低密度影,邻近肝S7段受压,增强后与对侧肾上腺比较呈相对低强化,其内囊性结构未见明确强化。左侧肾上腺、双肾形态、大小、密度未见异常,增强未见异常强化。肝脏形态、大小、各叶比例未见明确异常。肝实质密度均匀,未见明确异常密度影,未见明确异常强化。肝内、外胆管未见明显扩张。门静脉主干及左、右支,下腔静脉,肝静脉未见明显异常。胆囊形态、大小未见明确异常,胆囊壁未见明显增厚,腔内未见异常密度影。胰腺形态大小、密度未见异常,未见明确异常强化,胰周脂肪间隙清晰,胰管未见明显扩张。脾脏前方、内前方见两枚结节,平扫及增强同脾脏相似;脾脏形态、大小、密度未见明确异常,未见明确异常强化。肠曲分布及形态未见异常。腹膜后未见明确增大淋巴结。未见腹水征。结论:右侧肾上腺区结节,考虑良性肿瘤性病变可能性大。如图1。

图1 箭头处可见右侧肾上腺区见一类圆形结节,大小约25 mm×19 mm,边界清,平扫内见一囊状低密度影,邻近肝S7段受压,增强后与对侧肾上腺比较呈相对低强化
10月17日施行“腹腔镜右肾上腺肿瘤切除术”,术后病理诊断:肝肿物,由一些上皮样细胞构成,细胞胞浆丰富,红染或透亮,呈条索状、巢状或腺样排列,混杂少量血管样结构,免疫组化:CD31(+)、CD34(+)、FLi-1(+)、ERG(+)、S-100 部分(+)、Actin部分(+)、CK少数(+)、Ki67约5%(+)、Hepatocyte(-)、GPC3(-)、Desmin(-)、HMB45(-)、MelanA(-),符合肝上皮样血管内皮瘤,伴出血及坏死,侵犯肝被膜;周围肝组织汇管区见一些淋巴细胞浸润。结果如图2。
截止至2019年6月,患者定期复查未见复发及其他转移。
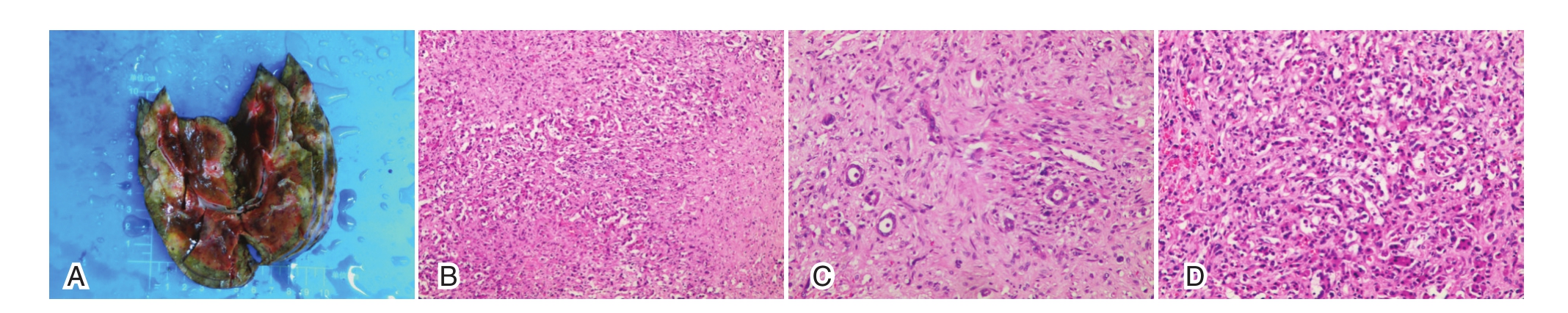
图2 手术大体病理及镜下HE染色图片
A大体病理图片;图B~D为镜下HE染色图片,可见该病理组织由一些上皮样细胞构成,细胞胞浆丰富,红染或透亮,呈条索状、巢状或腺样排列,混杂少量血管样结构,符合肝上皮样血管内皮瘤,伴出血及坏死,侵犯肝被膜;周围肝组织汇管区见一些淋巴细胞浸润
HEHE是一种介于血管瘤和血管肉瘤的潜在恶性的低度恶性肿瘤,HEHE于1984年由Ishak等[2]首次报道,而上皮样血管内皮瘤(epithelioid hemangioendothelioma,EHE)可发生于全身各处,有学者[3]回顾性分析了1994~2013年文献报道的239例EHE,发现该疾病患者的男女比例为1:1.91,年龄4~78岁,平均年龄39.6岁,可发生与全身各个部位,而发生于肝脏的HEHE则更为罕见。范飞等[4]分析了第二军医大学东方肝胆外科医院15例HEHE,发现男女比例为1∶2,这与EHE比例相近,发病年龄为20~80岁。该肿瘤的发病原因不明,发病机制尚不清楚,其临床表现特异性差,表现为单发或多发[5,6],患者常于肿瘤压迫神经、肝组织、胆管产生症状而就诊,部分患者于体检时发现。本例患者因腰背部间歇性疼痛,劳累加剧入院检查,由于肿瘤处于肾上腺区,初始考虑为肾上腺良性肿瘤。
HEHE虽然非常罕见,但具有一定的影像特征,尽管HEHE不能单纯依靠影像学确诊,国内部分学者对HEHE的影像特征已有部分研究和总结。宁周雨等[7]收集5例复旦大学附属肿瘤医院的HEHE,其报道了HEHE在B超表现为等低回声,在CT平扫表现为等低密度,MR平扫为低T1高T2信号,CT/MR增强扫描时病灶呈“慢进慢出”式明显、环状强化特点,PET/CT为明显高FDG摄取,且呈延迟显像的特点。徐亚丹等[8]回顾性分析了复旦大学附属中山医院11例HEHE的超声造影(CEUS)与增强CT两种检查的增强表现特点,总结出两种检查的特征表现,包括环形强化、整块强化及在各期相的强化特点,HEHE强化方式不一。赵桂玖等[9]回顾性分析8例经病理证实的肝脏EHE,均为多发病灶,包膜下生长,大小不一,有6例显示特征表现“包膜回缩征”和“棒棒糖征”,而周丽莎等[10]搜集经手术或穿刺活检后病理证实的HEHE11例,均为多发包膜下生长病灶,低密度或更低密度,强化方式与病灶的大小相关,亦有6例具“包膜回缩征”和“棒棒糖征”。刘露等[11]分析了四川大学华西医院15例经病理证实的HEHE,提出了HEHE的三种特征影像征象,包括其中13例见“肝包膜回缩征”,14例见“棒棒糖征”,7例见“核心模式”。赵越等[12]回顾分析了10例经病理证实的HEHE,总结了“包膜皱缩征”、“晕环征”、“棒棒糖征”、“瘤内血管征”等征象,并强调了“棒棒糖征”或“瘤内血管征”的特异性。朱璐珑等[13]回顾性分析了18例HEHE的MRI资料,发现DWI呈高信号,病灶ADC值范围为(1.58±0.25)×10-3 mm2/s,而正常肝组织 ADC 范围为(1.34±0.12)×10-3mm2/s,P<0.05,有统计学差异。本例患者肿瘤大小约25 mm×19 mm,CT增强检查表现为低密度,低强化,与文献报道的相符。
HEHE的临床表现和影像学表现均无特异性表现,极易误诊,目前病理和免疫组化是确诊HEHE的唯一方法。钟岚等[14]回顾性分析四川大学华西医院确诊为肝脏EHE的9例患者的病理组织学特点,镜下见肿瘤呈巢状、条索状排列,瘤细胞由梭形细胞、上皮样细胞、组织细胞样细胞或印戒样细胞构成,常形成胞质内血管,管腔内可见红细胞,肿瘤间质由黏液玻璃样变的纤维硬化区构成,瘤细胞浸润周围肝组织;免疫组织化学检测见肿瘤细胞FⅧ、CD34、CD31等内皮细胞表达阳性。本例患者病理组织由一些上皮样细胞构成,细胞胞浆丰富,红染或透亮,呈条索状、巢状或腺样排列,混杂少量血管样结构,免疫组化CD31、CD34阳性,这些与钟岚等报道的病理组织特点相符合。吕鹏等[15]总结10例复旦大学附属中山医院经病理证实的HEHE,发现10例CD34全部阳性,5例CD31阳性,4例FVIIIRAg阳性。另外,有学者[16]认为D2-40在肿瘤中有一定的阳性表达,是鉴别诊断中有价值的标记物。
由于HEHE是一种非常罕见的疾病,目前对HEHE的治疗方案尚无达成共识的治疗方案。其治疗方案包括肝切除手术、肝移植手术、放化疗、免疫治疗、经皮穿刺肝动脉栓塞等。Grotz等[17]回顾性分析了1984~2007年在美国梅奥诊所接受治疗的30例HEHE患者,其中11例接受了肝切除手术,术后5年存活率为86%;11例接受肝移植手术,术后5年存活率为73%。作者认为肝切除手术适用于可切除疾病和有利预后因素的患者,肝移植手术适用于无法切除的疾病患者,也可能适用于预后不良的患者。对于不能肝切除手术的患者,肝移植手术效果显著[18]。美国器官资源共享网络(UNOS)统计了1987~2005年间接受肝移植手术治疗的110例HEHE患者,术后5年存活率达64%[19]。李建军等[20]分析了首都医科大学附属北京佑安医院4例经肝动脉栓塞TAE联合微波消融MWA治疗的HEHE患者,其中一例不按期复查,最后随访52个月后发现复发,其他4例未见复发,其中报道随访时间最长为35个月,最短为12个月。然而,Thomas等[21]对单一学术癌症中心在1989年至2013年间的50例HEHE患者进行回顾性分析,发现与未接受任何化疗的患者相比,在疾病过程中任何时间接受化疗的患者的5年生存率均降低,其认为HEHE经常遵循惰性过程,提示立即治疗可能不是最佳策略。HEHE是一种介于血管瘤与血管肉瘤之间的低度恶性肿瘤,其预后差异大,取决于肿瘤大小、数目、部位、有无转移、治疗方案等,但治疗效果明显优于肝癌。对可行肿瘤切除和肝移植手术患者应尽早手术治疗,预后与个体差异关系大,有的患者可以表现为惰性过程,值得注意的是有的患者表现为转移,但却可以带瘤生存多年。
总之,由于HEHE十分罕见,临床表现与影像特征特异性差,容易误诊,病理组织是唯一确诊的方法,治疗以肝肿物切除与肝移植手术为主。
[1] Treska V,Daum O,Svajdler M,et al.Hepatic Epithelioid He-mangioendothelioma-a Rare Tumor and Diagnostic Dilemma[J].In vivo(Athens,Greece),2017,31(4):763-767.
[2] Ishak KG.Epithelioid hemangioendothelioma of the liver:a clin-icopathologic and follow-up study of 32 cases[J].Hum Pathol,1984,15(9):839-852.
[3] 杨文博.上皮样血管内皮瘤239例文献分析[J].中国实用内科杂志,2015,35(S1):28-30.
[4] 范飞,黄斌,俞文隆,等.肝脏上皮样血管内皮瘤临床影像特征(附15例分析)[J].第二军医大学学报,2014,35(7):811-813.
[5] 马风荣,周刚,李霞,等.弥漫性肝脏上皮样血管内皮瘤影像表现一例[J].临床放射学杂志,2017,36(9):1341-1342.
[6] Gan LU,Chang R,Jin H,Yang LI.Typical CT and MRI signs of hepatic epithelioid hemangioendothelioma[J].Oncol Lett,2016,11(3):1699-1706.
[7] 宁周雨,陈其文,朱晓燕,等.肝脏上皮样血管内皮瘤的影像特点及临床诊治体会[J].中国癌症杂志,2016,26(12):1004-1011.
[8] 徐亚丹,王文平,王希,等.肝上皮样血管内皮瘤的超声造影和增强CT表现[J].中国医学影像学杂志,2017,25(6):452-456.
[9] 赵桂玖,王庆兵,曾蒙苏,等.肝上皮样血管内皮瘤的CT和MRI表现[J].中国临床医学影像杂志,2015,26(8):577-580.
[10] 周丽莎,翟凤仪,董帜,等.肝脏上皮样血管内皮瘤的CT和MRI表现[J].临床放射学杂志,2015,34(3):402-405.
[11] 刘露,鲁亚,刘曦娇,等.肝上皮样血管内皮细胞瘤的影像学表现[J].中国普外基础与临床杂志,2018,25(2):229-234.
[12] 赵越,龙世亮,田执南,等.肝上皮样血管内皮瘤的CT与MRI特征及病理基础[J].CT理论与应用研究,2015,24(4):563-569.
[13] 朱璐珑,曹代荣,王明亮,等.肝脏上皮样血管内皮瘤MRI征象[J].中国医学影像技术,2018,34(7):1046-1049.
[14] 钟岚,张秀辉,何度,等.肝上皮样血管内皮瘤9例临床病理分析及文献复习[J].中国普外基础与临床杂志,2015,22(2):224-229.
[15] 吕鹏,林江,周易,等.肝脏上皮样血管内皮瘤:影像表现和病理基础[J].中国医学计算机成像杂志,2011,17(5):416-419.
[16] Fujii T,Zen Y,Sato Y,et al.Podoplanin is a useful diagnostic marker for epithelioid hemangioendothelioma of the liver[J].Mod Pathol,2008,21(2):125-130.
[17] Grotz TE,Nagorney D,Donohue J,et al.Hepatic epithelioid haemangioendothelioma:is transplantation the only treatment option[J]?HPB,2010,12(8):546-553.
[18] Fukuhara S,Tahara H,Hirata Y,et al.Hepatic epithelioid he-mangioendothelioma successfully treated with living donor liver transplantation:A case report and literature review[J].Clin Case Rep,2019,8(1):108-115.
[19] Rodriguez JA,Becker NS,O'Mahony CA,et al.Long-Term Outcomes Following Liver Transplantation for Hepatic Heman-gioendothelioma:The UNOS Experience from 1987 to 2005[J].J Gastrointest Surg,2008,12(1):110-116.
[20] 李建军,朱桐,杨晓珍,等.肝上皮样血管内皮瘤肝动脉栓塞联合微波消融治疗效果初步分析(附4例报告)[J].北京医学,2017,39(12):1209-1212+1327.
[21] Thomas RM,Aloia TA,Truty MJ,et al.Treatment sequencing strategy for hepatic epithelioid haemangioendothelioma [J].HPB(Oxford),2014,16(7):677-685.
Hepatic epithelioid hemangioendothelioma:a case report and review of literature
中图分类号: